박테리아 치료를 위한 신규 항생제 개발 비용이 증가함에도 내성 발현 속도가 더욱 빨라지면서 사용이 어려워지고 있다.
특히 두 가지 이상이 항생제에 내성을 갖는 슈퍼박테리아 증가로 기존 치료법의 한계가 명확해지고 있다.
이에 세계보건기구(WHO)는 슈퍼박테리아가 차세대 팬데믹을 가져올 것을 경고하는 등 새로운 항균 치료법의 개발이 시급한 상황이다.
바이오나노기술로 슈퍼박테리아 해결
한국생명공학연구원(이하 생명연) 감염병연구센터 류충민 박사팀이 바이오나노기술을 이용해 슈퍼박테리아를 효과적으로 제어할 수 있는 금나노입자·지질나노입자 기반 신규 항생제를 개발했다.
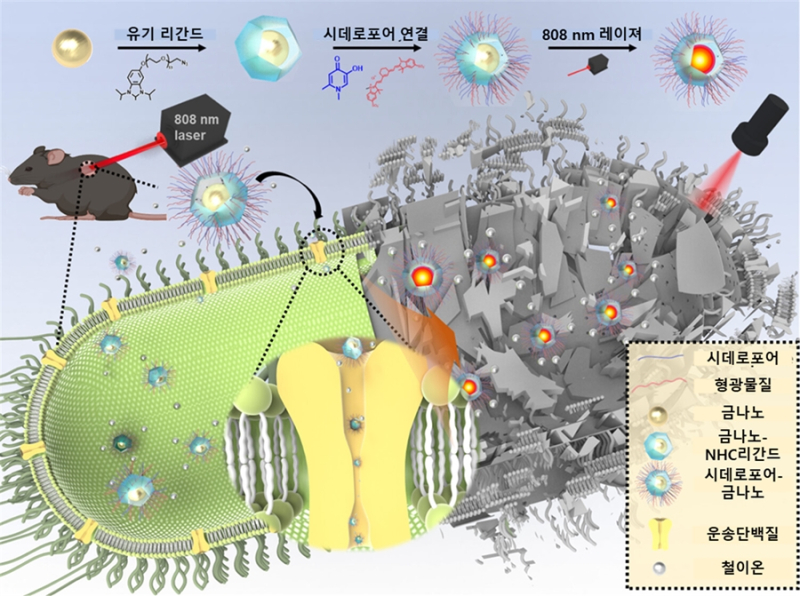
연구팀은 세균 생존에 필요한 철분을 세포 내로 이동시키는 유기물질 ‘시데로포어’에 금나노입자를 결합하고 808㎚ 파장의 근적외선을 비췄다.
이 결과 세균 속에 들어간 금나노입자가 순간적으로 수백 ℃ 열을 발생시켜 실험대상인 녹농균을 물리적으로 사멸시켰다.
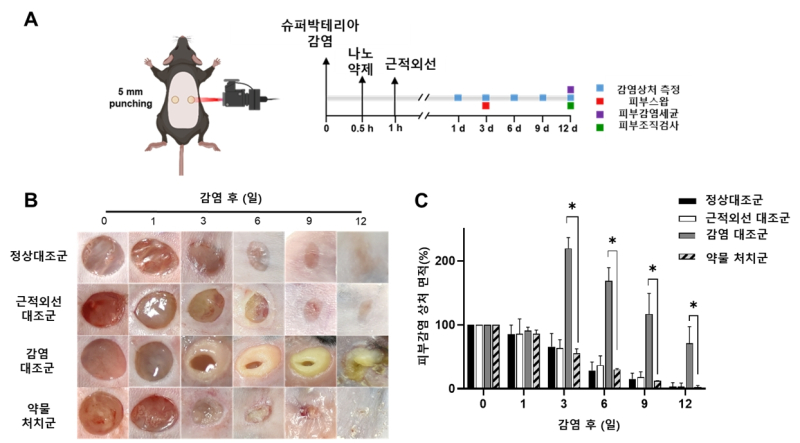
실제 피부감염 생쥐를 이용한 실험에서 신속하게 상처가 치유되고, 면역세포나 정상피부 조직에는 영향을 미치지 않아 높은 생체안전성을 보였다.
아울러 연구팀은 다른 연구에서 세균 내로 유전자 편집시스템(CRISPR-Cas13a)을 전달할 수 있는 새로운 지질나노입자를 제작했다.
신규 지질나노입자에 사용된 CRSIPR-Cas13a는 가이드 RNA가 세균의 특정 유전자를 인식하면 유전자 편집시스템에 있는 효소(Cas13a)가 세포 내 RNA를 무작위로 분해해 세균이 사멸했다. 세균을 사멸시킬 수 있다.
이를 패혈증 동물모델에 적용한 결과 새로운 지질나노입자에 의해 세균 몸으로 들어간 유전물질이 치명적인 유전자 편집을 일으켜 세균이 사멸하고 패혈증을 억제하는 것을 확인했다.

이 기술은 인체에 유익한 균에는 영향을 주지 않고 특정 병원균만 선택적으로 사멸시켜 항생제 내성 문제를 극복하면서 슈퍼박테리아를 제어하는 새로운 가능성을 연 것으로 평가된다.
류 박사는 “이번 연구는 기존 광범위 항생제와 달리 특정 슈퍼박테리아만 선택적으로 제거할 수 있어 인체의 정상 세균총에 미치는 영향을 최소화한 것이 특징”이라며 “추가 연구를 통해 슈퍼박테리아와의 싸움에서 중요한 전환점을 맞이할 수 있을 것으로 기대된다”고 말했다.
한편, 이번 연구성과는 지난 2월 2일 국제학술지 ‘ACS Nano(IF 15.8)’에 게재됐고, 지난달 14일 ‘Advanced Healthcare Materials(IF 10.0)’ 표지논문으로 실렸다.
(논문명 : Siderophore-Functionalized Nanodrug for Treating Antibiotic-Resistant Bacteria / 교신저자 : 생명연 류충민‧권오석 박사 / 제1저자 : 서휘원 박사, 하시영‧김진영 선임연구기사)
(논문명 : Lipid Nanoparticle-Mediated CRISPR-Cas13a Delivery for the Control of Bacterial Infection / 교신저자 : 생명연 류충민‧김다정 박사 / 제1저자 : 김부건 박사후연구원)











